ピーエイチ?ペーハー?
「pH」という言葉は、日常生活でもたくさん目にする事も多いかと思います。
現在では「ピーエイチ」と読むことが普通となっていますが、「ペーハー」とドイツ語流の読み方も多く認知されています。Pはドイツ語でPotenz(力・能力の意味)の略で、Hは水素の元素記号です。
つまり、pHは化学的にいうと、溶液中の水素イオン濃度 〔H+〕の量を表しており、日本語では「水素イオン指数」と訳します。
水溶液の性質を表す単位
人間の状態を表す単位に「体重=Kg」や「体温=℃」があるように、pHも水溶液の性質を表す一つの単位です。
pHが7より小さいと酸性、7より大きいとアルカリ性となります。
pHが水素イオン指数と訳されている事からもわかりますが、液体の酸性、アルカリ性は、その液体に溶けている水素イオンの量によって決まります。
純水な水の中には水素イオン(H+)と水酸化物イオン(OH-)が同じ量存在しています。
この状態を中性と呼びます。
pHが7より小さい場合、水素イオン濃度は中性の時よりも多くなる為、酸性となります。
pHが7より大きい場合、水素イオン濃度は中性のときよりも少なくなり、「アルカリ性」となります。
pHの指数はゼロから14まであり、ゼロに近づくほど酸性の度合いが高くなり、14に近づくほどアルカリ性の度合いが高くなります。
酸性の水溶液は「なめると酸(す)っぱい」という特徴があります。酸性の水溶液の名前には「酸」という文字が含まれるので、わかりやすい液性です。
アルカリ性の水溶液は、「なめると苦いまたは渋い」という特徴があります。
中性の水溶液は味もさまざまで、砂糖水は甘く、塩水はしょっぱく感じます。
まとめ
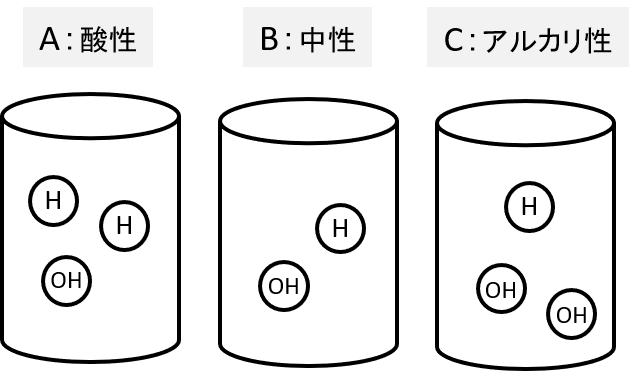
下図で「H」は水素、「O」は酸素を示し、「OH」は水素と酸素が合わさった「水酸基」と呼ばれます。これらは水の中では電気を帯びた「イオン」という状態(H+とOH-)で存在し、前著した通り、水溶液のpHは水素イオン(H+)濃度によって決まります。
図Aは「H+」が「OH-」よりも多い酸性の状態、図Bは「H+」と「OH-」が同数で中性の状態、図Cは「H+」が「OH-」よりも少ないアルカリ性の状態を示しています。
【pH中和処理でお困りのお客様はお気軽に】